Wir beschäftigen uns mit verschiedenen Arten von Zellen, Batterien und Energiespeichersystemen.
Bei Fragen zu unseren Produkten hinterlassen Sie uns bitte eine Nachricht, wir melden uns innerhalb von 24 Stunden bei Ihnen.

Wir beschäftigen uns mit verschiedenen Arten von Zellen, Batterien und Energiespeichersystemen.
Bei Fragen zu unseren Produkten hinterlassen Sie uns bitte eine Nachricht, wir melden uns innerhalb von 24 Stunden bei Ihnen.
Falls Sie sich jemals gefragt haben, warum Lithium-Ionen-Batterien in Smartphones und Elektrofahrzeugen verwendet werden, liegt die Antwort in ihrer unglaublichen Energiedichte.
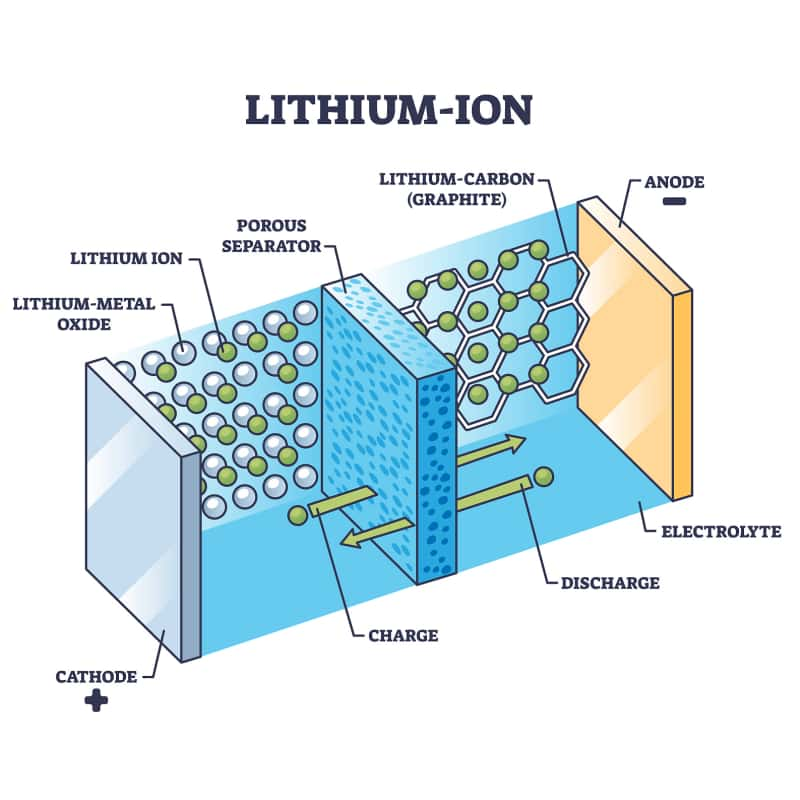
Man kann sich eine Batterie als ein System mit zwei getrennten Behältern für „Energieteilchen“ (Lithiumionen) vorstellen.LadenDabei werden die Partikel von einem Tank in den anderen befördert, wodurch Energie gespeichert wird.Entladunglässt sie zurückfließen und setzt so diese Energie frei, um Ihr Gerät mit Strom zu versorgen.
Anode (negative Elektrode):Üblicherweise hergestellt ausGraphit(Kohlenstoff). Dies ist der „Tank“, in dem Lithium-Ionen gespeichert werden, wenn die Batterie geladen wird.
Kathode (positive Elektrode):Hergestellt aus einem Lithiummetalloxid (wie Lithium-Cobalt-Oxid oder Lithium-Eisenphosphat). Dies ist der andere „Tank“.
Welche Rolle spielt der Elektrolyt in einer Lithium-Ionen-Batterie?:Eine Flüssigkeit oder ein Gel, das sich zwischen Anode und Kathode befindet. Es ermöglichtLithiumionenum hindurchzukommen, aber BlöckeElektronen(Das ist entscheidend!).
Separator:Eine poröse Membran im Inneren des Elektrolyten verhindert, dass sich Anode und Kathode berühren (was einen Kurzschluss verursachen würde).
Externer Schaltkreis:Der Draht oder die Leitung, die Anode und Kathode außerhalb der Batterie verbindet. Hier befindet sich der Anschluss.ElektronenDer Stromfluss versorgt Ihr Gerät mit Strom.
Wenn Sie Ihr Gerät einschalten, schließen Sie den Stromkreis, und eine chemische Reaktion setzt spontan ein.
Lithium-Ionen-Reisen:Lithiumionen, die in derGraphitanodesich ablösen und durchschwimmenElektrolytzumKathode.
Elektronen nehmen den malerischen Weg:Für jedes Ion, das sich bewegt, wird ein Elektron von der Anode freigesetzt. Der Elektrolyt blockiert die Elektronen, sodass sie gezwungen sind, den Weg über die Anode zu nehmen.externer Stromkreis(durch die Komponenten Ihres Telefons) zur Kathode zu gelangen. Dieser Elektronenflussist Elektrizität, um Ihr Gerät mit Strom zu versorgen.
Wiedervereinigung:An der Kathode vereinigen sich die Elektronen und Lithiumionen wieder und lagern sich in das Kathodenmaterial ein.
Entlassungsbericht:Anode (Graphit + Li)→Elektronen (Leistungsgerät) + Li⁺ (über Elektrolyt)→Kathode (Li rekombiniert)
Energie wird freigesetzt.
Durch das Einstecken wird eine externe elektrische Kraft angelegt, die das System in die umgekehrte Richtung drückt.
Externe Energie treibt Elektronen an:Das Ladegerät zwingt Elektronen zum Fluss.zurückvon der Kathode zur Anode.
Lithium-Ionen folgen:Dadurch werden die Lithiumionen aus dem Kathodenmaterial herausgezogen und gezwungen, durch den Elektrolyten zurück zur Anode zu schwimmen.
Lagerung:Die Ionen lagern sich wieder in die Graphitstruktur der Anode ein und sind somit bereit für den nächsten Entladezyklus.
Zusammenfassung der Gebühren:Kathode (Li)→Li⁺ (durch das Ladegerät durch den Elektrolyten gepresst)→Anode (Graphit + Li)
Energie wird gespeichert.
Stellen Sie sich ein Wasserrad vor, das eine Mühle antreibt:
Der angeklagte Staat:Das gesamte Wasser (Lithiumionen) befindet sich imoberer Eimer (Anode)Dies stellt gespeicherte Energie dar.
Entladung:Man öffnet das Tor. Wasser fließt vom oberen Eimer nach unten durch die...Wasserrad (Ihr Gerät), in dieunterer Eimer (Kathode)Das sich drehende Wasserrad funktioniert.
Aufladen:Sie verwenden eine Pumpe (Ihr Ladegerät), um das Wasser aus dem unteren Eimer wieder nach oben in den oberen Eimer zu befördern und so erneut Energie zu speichern.
Eine Nachricht hinterlassen
Scannen zu Wechat :

Hi! Click one of our members below to chat on